Bài viết có sự tham vấn chuyên môn của Tiến sĩ Trịnh Như Thùy – Giám đốc Ngân hàng mô – tế bào gốc DNA
Đái tháo đường týp 2 có thể gây biến chứng nguy hiểm như tim mạch, suy thận, tổn thương thần kinh và mắt. Liệu pháp tế bào gốc trung mô (MSC) hứa hẹn không chỉ kiểm soát đường huyết mà còn tái tạo và phục hồi chức năng các tế bào beta tuyến tụy.
1. Bệnh đái tháo đường típ 2 và tế bào gốc trung mô (MSC)
Đái tháo đường típ 2 là một bệnh lý mạn tính do rối loạn chuyển hóa glucose trong cơ thể, gây ra bởi tình trạng kháng insulin hoặc suy giảm tiết insulin từ tế bào beta trong tuyến tụy. Trong tình trạng này, cơ thể không sử dụng insulin một cách hiệu quả, dẫn đến lượng đường trong máu tăng cao. Bệnh này đang trở thành một vấn đề y tế toàn cầu, ảnh hưởng nghiêm trọng đến sức khỏe và chất lượng cuộc sống của hàng triệu người, đồng thời dẫn đến nhiều biến chứng nguy hiểm nếu không được điều trị hiệu quả. Các phương pháp điều trị hiện nay, bao gồm chế độ ăn uống, tập luyện và thuốc, tuy giúp kiểm soát mức đường huyết nhưng chưa thể điều trị triệt để hoặc ngăn ngừa sự suy giảm chức năng tụy.
Đái tháo đường týp 2 có thể dẫn đến nhiều biến chứng nguy hiểm như bệnh tim mạch, suy thận, tổn thương thần kinh và các vấn đề về mắt nếu không được kiểm soát tốt. Liệu pháp điều trị bằng tế bào gốc trung mô (MSC) là một phương pháp đầy hứa hẹn, không chỉ tập trung vào việc kiểm soát đường huyết mà còn nhắm đến tái tạo và phục hồi chức năng của các tế bào beta trong tuyến tụy. Tế bào gốc trung mô, với khả năng phân chia, biệt hóa và điều hòa miễn dịch, đã được chứng minh có thể giảm viêm, giảm tính kháng insulin ở các mô, cải thiện chức năng của tuyến tụy và tăng cường sản xuất insulin của cơ thể.
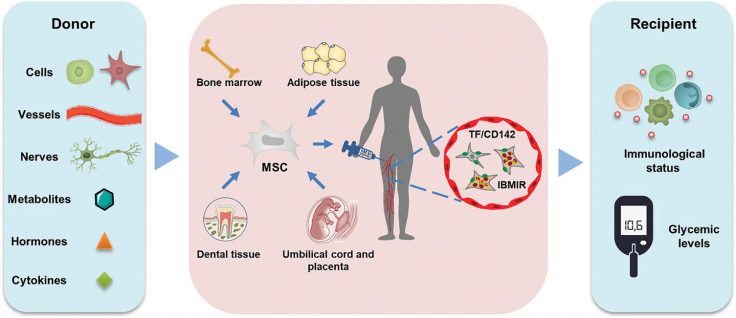
MSC đã được phân lập thành công từ nhiều loại mô/cơ quan, bao gồm tủy xương, mô mỡ, mô răng, dây rốn và nhau thai. Các tế bào MSC này có khả năng điều hoà miễn dịch và mức đường huyết (glycemic levels) của người nhận. MSC có các protein màng bề mặt tế bào có vai trò quan trọng trong quá trình đông máu (TF/CD142), một tác nhân chính gây ra phản ứng viêm tức thời, tạo nên phản ứng miễn dịch bẩm sinh (IBMIR) điều chỉnh đáp ứng miễn dịch của cơ thể người nhận khi được ghép.
2. Các cơ chế sinh lý bệnh chính dẫn đến sự phát triển của bệnh đái tháo đường típ 2
Các yếu tố nguy cơ bao gồm lối sống ít vận động, béo phì, tiền sử gia đình, tuổi tác, tiền đái tháo đường, hội chứng buồng trứng đa nang (PCOS) và huyết áp cao. Những yếu tố này góp phần vào rối loạn chức năng của tế bào beta trong tuyến tụy.
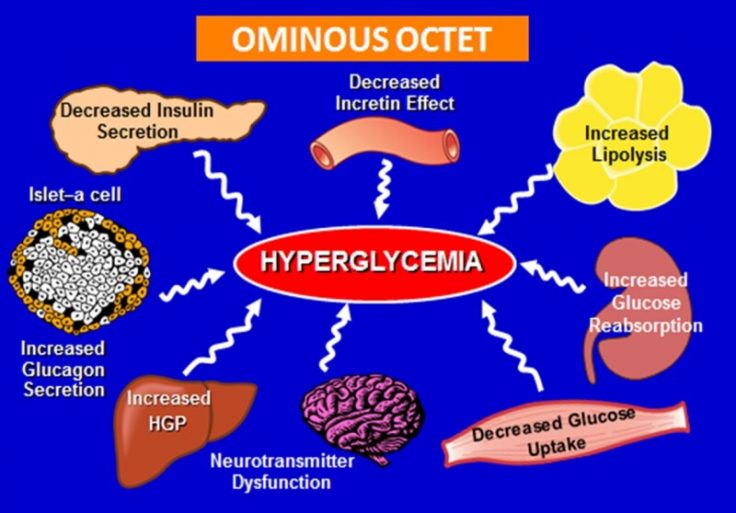
Rối loạn chức năng tế bào beta gây giảm bài tiết insulin, một hormone quan trọng trong việc điều hòa nồng độ glucose trong máu. Khi lượng insulin tiết ra giảm, nồng độ glucose trong máu sẽ tăng cao, dẫn đến tình trạng tăng đường huyết (hyperglycemia).
Bên cạnh đó, các yếu tố nguy cơ còn làm gia tăng sản xuất axit béo và gây ra tình trạng kháng insulin, tức là các tế bào không đáp ứng hiệu quả với insulin. Sự kháng insulin dẫn đến việc tăng tiết glucose và làm giảm khả năng hấp thu glucose ở cơ, mô mỡ, gan, não,…làm tình trạng tăng đường huyết trở nên nghiêm trọng hơn:
– Tình trạng kháng insulin ở gan: Gan là cơ quan quan trọng sản xuất glucose trong thời gian nhịn ăn. Ở bệnh đái tháo đường típ 2, tế bào gan kháng insulin, tức là gan sản xuất glucose một cách không kiểm soát mặc dù có sự hiện diện của insulin hoặc không dẫn đến tăng lượng đường trong máu lúc đói.
– Tình trạng kháng insulin ở mô mỡ: Ở những bệnh nhân béo phì hoặc gan nhiễm mỡ, tình trạng kháng insulin của mô mỡ dẫn đến tăng phân giải lipid của mô mỡ, từ đó sản xuất ra nhiều glycerin và triglyceride, hai chất tạo thành đường khi di chuyển đến các tế bào gan.
– Tình trạng kháng insulin ở cơ: Khi các cơ hoạt động, chúng sử dụng glucose nhờ tác động của insulin. Khi tình trạng kháng insulin xảy ra ở các tế bào cơ, glucose không thể hoạt động, dẫn đến tình trạng không có năng lượng, làm cho lượng glucose trong máu cao.
Sự gia tăng glucose và axit béo trong máu cũng ảnh hưởng đến hệ thống miễn dịch, làm suy giảm đáp ứng miễn dịch của cơ thể. Kết hợp tất cả các yếu tố này, quá trình tăng đường huyết không được kiểm soát sẽ dẫn đến sự tiến triển của bệnh đái tháo đường típ 2, làm tăng nguy cơ gặp phải các biến chứng lâu dài như bệnh tim mạch, tổn thương thận, và các vấn đề về thần kinh.
3. Hiệu quả của tế bào gốc trung mô đối với bệnh đái tháo đường típ2.
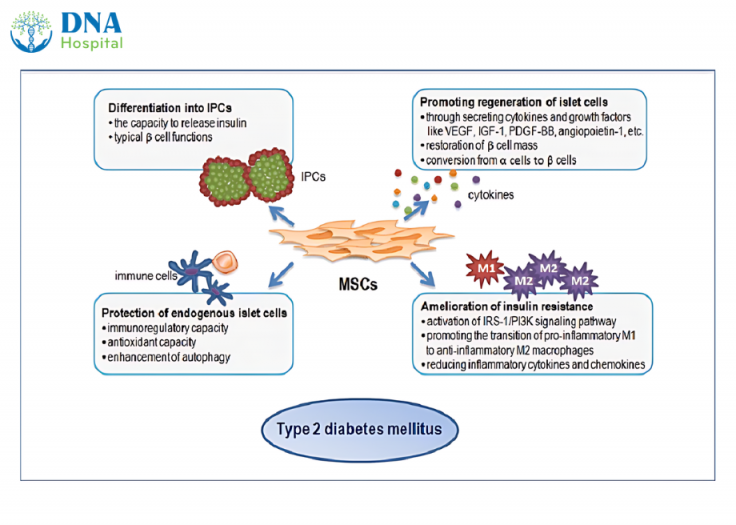
Biệt hoá thành tế bào tiết insulin: là một trong những cơ chế chính đầu tiên của MSC trong việc hạ đường huyết trên bệnh nhân đái tháo đường típ 2. Cơ chế biệt hoá thành các tế bào nội tiết trong tụy được điều khiển bởi các yếu tố như Pdx-1, Ngn-3, Neuro-D1, Pax4 và Pax6. Với việc biết chính xác các yếu tố thúc đẩy quá trình biệt hoá sẽ giúp rất nhiều cho việc tái lập chương trình thúc đẩy tế bào tiền thân hay tế bào gốc thành MSC tiết insulin.
Thúc đẩy tái tạo của tế bào tiền thân tụy: MSC còn có khả năng thúc đẩy sự tái tạo của tế bào tiền thân beta bằng cách di cư tới vùng tụy đảo có tế bào bị tổn thương. Thực hiện quá trình này, MSC sẽ tiết ra nhiều loại cytokines và nhân tố phát triển sau một hay nhiều lần ghép MSC; tạo ra một vi môi trường mà nhờ đó các tế bào tiền thân nội sinh sẽ tăng sinh và biệt hoá thành tế bào beta trưởng thành, giúp điều hòa đường huyết.
Bảo vệ tế bào beta nội sinh: MSC có đặc tính điều hoà miễn dịch và được biết đến như một tế bào có ưu thế về miễn dịch khi biểu hiện thấp MHC lớp II và các phân tử đồng kích thích (MHC là phân tử tương hợp mô giúp nhận biết tế bào lạ và quen trong cơ thể người). Là một thành phần chính của miễn dịch thu được, lympho T đóng vai trò quan trọng trong các bệnh tự miễn và phản ứng thải ghép. Các nghiên cứu chỉ ra rằng, MSC ức chế sự tăng sinh lympho T bằng cách ức chế sự chuyển hoá năng lượng của lympho T, thúc đẩy sự dung nạp lympho T hoặc làm tăng số lượng T điều hoà (được biết đến như một loại tế bào ức chế lympho T gây độc hoạt động, còn gọi là tế bào T cytotoxic hoặc CD8+ T cells), MSC có thể ức chế hoạt động của các tế bào T gây độc và điều hoà hệ miễn dịch để giảm phản ứng miễn dịch quá mức, giúp bảo vệ tế bào beta tuyến tuỵ trong bệnh đái tháo đường típ 2. Hơn nữa, MSC còn có khả năng ức chế sự tăng sinh lympho B và giảm các chức năng của các tế bào miễn dịch khác như: T gây độc, tế bào tiêu diệt tự nhiên và các cytokines hay các phân tử có chức năng miễn dịch. Chính hiệu quả ức chế miễn dịch trên các tế bào miễn dịch làm giảm nhẹ quá trình tự miễn, dẫn tới làm giảm sự phá huỷ tế bào beta tuyến tụy.
Giảm sự đề kháng insulin: rối loạn chức năng tiết insulin và đề kháng insulin là 2 tình trạng cùng tồn tại song song ở bệnh nhân đái tháo đường típ 2. Do đó, việc điều trị hiệu quả đái tháo đường típ 2 không thể chỉ bằng khôi phục hay cải thiện sự sản xuất insulin của tuyến tụy. Sự đề kháng insulin hiện nay được xem có quan hệ chặt chẽ với tình trạng viêm mức độ thấp toàn thân. Cytokines và các chất hóa hướng động như tumor necrosis factor alpha (TNF-α), interleukin-1 beta (IL-1β) được sản xuất bởi đại thực bào tại mô mỡ trong pha M1 tiền viêm được xem như là các yếu tố chủ yếu để khởi động quá trình viêm và khuếch đại sự đề kháng insulin. Phân tử kháng viêm từ đại thực bào gọi là M2 được chứng minh có tác dụng giảm sự đề kháng insulin. MSC có khả năng biểu hiện hiệu quả kháng viêm bằng cách chuyển phân cực đại thực bào từ M1 sang M2.
4. Tính an toàn, hiệu quả và ứng dụng lâm sàng của tế bào gốc trung mô trong điều trị bệnh đái tháo đường típ 2.
Các nghiên cứu gần đây cho thấy MSC có thể giúp giảm đường huyết, cải thiện độ nhạy insulin và hỗ trợ điều chỉnh hệ miễn dịch cho bệnh nhân đái tháo đường típ 2. MSC đã được ứng dụng trong thử nghiệm lâm sàng với những kết quả tích cực về kiểm soát đường huyết và chức năng của tuyến tụy, đặc biệt là các tế bào beta sản xuất insulin.
Mặc dù MSC có tiềm năng lớn trong y học tái tạo, các thách thức như tính dị biệt của tế bào và nguy cơ kích hoạt miễn dịch vẫn là rào cản đối với ứng dụng lâm sàng. Những nghiên cứu lâm sàng trước đây đã giúp làm rõ những vấn đề này. Đặc biệt, quy định về nguồn gốc MSC và đảm bảo an toàn thông qua các tiêu chuẩn sản xuất và thử nghiệm.
Kết quả từ sáu thử nghiệm lâm sàng sử dụng tế bào gốc trung mô (MSC) của Aanchal Mathur năm 2023 bao gồm 262 bệnh nhân đái tháo đường típ 2 và chứng minh rằng MSC an toàn khi sử dụng và không biểu hiện bất kỳ tác dụng phụ nghiêm trọng nào. MSC biểu hiện khả năng sinh miễn dịch thấp do một nhóm protein bề mặt đóng vai trò quan trọng trong hệ miễn dịch MHC 1 (Major Histocompatibility Complex class I) và 2 thấp không gây ra sự hoạt hóa của tế bào lympho. MSC an toàn hơn các liệu pháp thông thường được sử dụng để điều trị đái tháo đường típ 2. Hiệu quả của liệu pháp MSC được đo dựa trên mức HbAc1, C-peptide và Fasting Blood Glucose (FBG). Hầu hết các nghiên cứu đều áp dụng thời gian theo dõi là 12 tháng sau một liều MSC. Phương pháp điều trị MSC đã chứng tỏ là giải pháp lâu dài cho hầu hết các trường hợp. Mức C-peptide vẫn bình thường trong 12 tháng sau khi tiêm. Mức FBG và HbAc1 thay đổi trong các nghiên cứu khác nhau nhưng cải thiện ở 70% bệnh nhân.
Đường truyền MSC qua tĩnh mạch hoặc qua động mạch tụy, không tạo ra sự khác biệt đáng kể về hiệu quả điều trị sau 3, 6 và 12 tháng theo dõi. Tất cả các nghiên cứu đều sử dụng MSC tự thân được tăng sinh cho 3–4 lần truyền. Số lượng tế bào MSC được cấy ghép cao cho phép giảm tần suất truyền so với phương pháp điều trị thông thường, người bệnh không cần phải truyền tế bào quá thường xuyên như các phương pháp khác. Đặc biệt trong những trường hợp bệnh tiến triển nặng, việc cấy ghép MSC có thể giúp giảm nhu cầu tiêm insulin hàng ngày hoặc ghép tạng (đối với các bệnh liên quan đến sự suy giảm chức năng của một cơ quan).
Tuy vậy, ứng dụng lâm sàng của liệu pháp MSC thường đối mặt với các thách thức khoa học và đạo đức, bao gồm nguy cơ kích hoạt miễn dịch. Để đảm bảo tính an toàn và hiệu quả, cần tuân thủ các tiêu chuẩn chọn lọc, nguồn gốc tế bào và quy định nghiêm ngặt. Điều này nhấn mạnh tầm quan trọng của việc nghiên cứu liên tục và cập nhật chính sách nhằm tối ưu hóa liệu pháp MSC cho các bệnh lý khác nhau, đặc biệt trong điều trị tiểu đường.
[1]. Ji Chen, Chen-Xi Zheng, Yan Jin, Cheng-Hu Hu. Mesenchymal Stromal Cell-Mediated Immune Regulation: A Promising Remedy in the Therapy of Type 2 Diabetes Mellitus. Stem Cells, Volume 39, Issue 7, July 2021, Pages 838-852, Doi.org/10.1002/stem.3357.
[2]. Mathur A, Taurin S, Alshammary S. The Safety and Efficacy of Mesenchymal Stem Cells in the Treatment of Type 2 Diabetes- A Literature Review. Diabetes Metab Syndr Obes. 2023 Mar 14;16:769-777. doi: 10.2147/DMSO.S392161. PMID: 36941907; PMCID: PMC10024492.
[3]. Galicia-Garcia U, Benito-Vicente A, Jebari S, Larrea-Sebal A, Siddiqi H, Uribe KB, Ostolaza H, Martín C. Pathophysiology of Type 2 Diabetes Mellitus. Int J Mol Sci. 2020 Aug 30;21(17):6275. doi: 10.3390/ijms21176275. PMID: 32872570; PMCID: PMC7503727.
[4]. Mou L, Wang TB, Wang X, Pu Z. Advancing diabetes treatment: the role of mesenchymal stem cells in islet transplantation. Front Immunol. 2024 Mar 28;15:1389134. doi: 10.3389/fimmu.2024.1389134. PMID: 38605972; PMCID: PMC11007079.
[5]. Solis-Herrera C, Triplitt C, Cersosimo E, et al. Pathogenesis of Type 2 Diabetes Mellitus. [Updated 2021 Sep 27]. In: Feingold KR, Anawalt B, Blackman MR, et al., editors. Endotext [Internet]. South Dartmouth (MA): MDText.com, Inc.; 2000-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK279115/.
[6]. Zang L, Hao H, Liu J, Li Y, Han W, Mu Y. Mesenchymal stem cell therapy in type 2 diabetes mellitus. Diabetol Metab Syndr. 2017 May 15;9:36. doi: 10.1186/s13098-017-0233-1. PMID: 28515792; PMCID: PMC5433043.











